自身免疫性葡萄膜炎(Autoimmune uveitis, AU)是导致工作年龄人群失明的重要原因之一,传统治疗依赖糖皮质激素,但效果有限且常伴有股骨头坏死、血糖异常等严重副作用;新型生物制剂虽有一定疗效,但价格昂贵,许多患者难以负担。由香港浸会大学、香港大学、上海交通大学医学院等多家机构共同完成的一项最新研究,揭示了一条全新的治疗路径。该研究於2026年3月在国际权威期刊《Cell Death & Differentiation》线上正式发表。
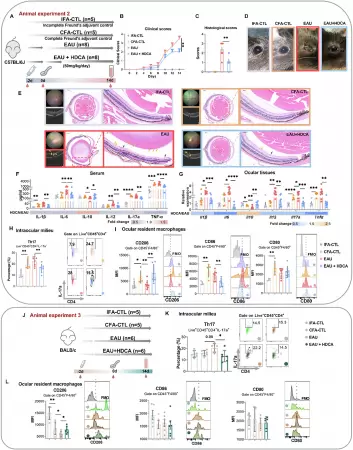
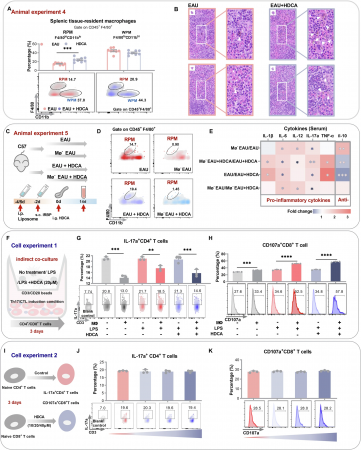
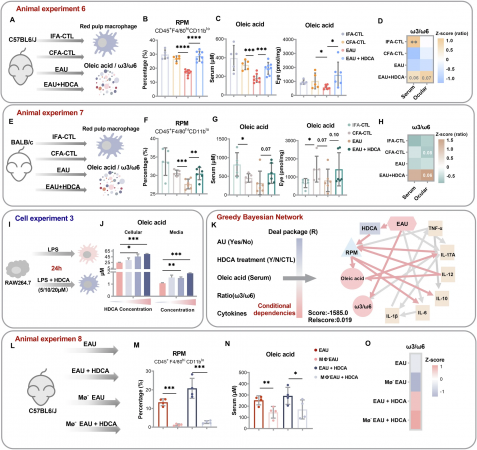
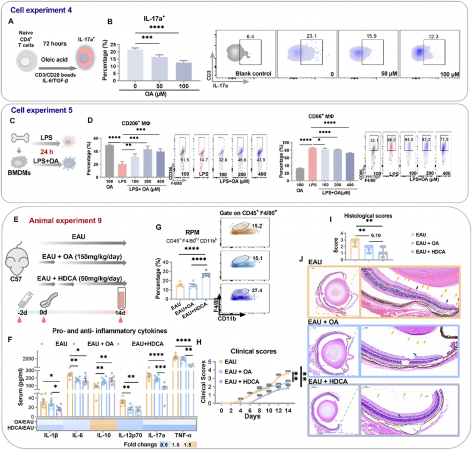
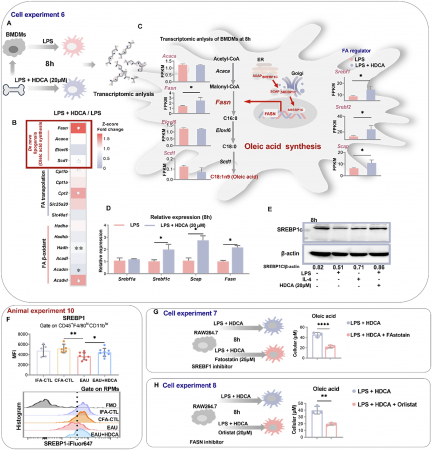
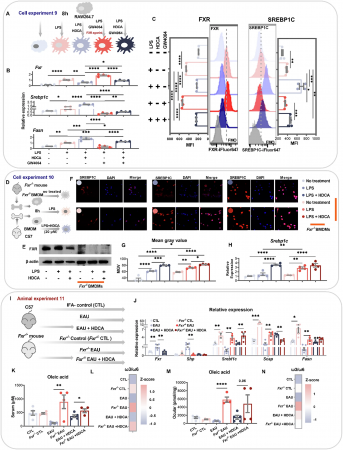
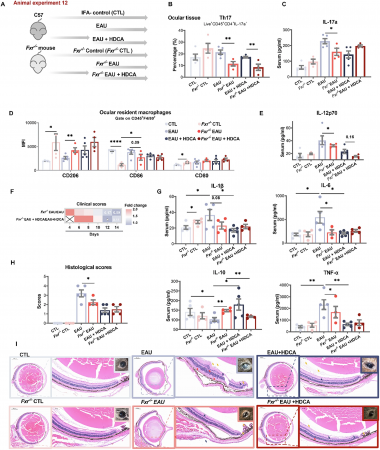
研究团队通过对90名临床参与者的血清代谢组学分析,首次发现AU患者体内肠道来源的次级胆汁酸——猪去氧胆酸(HDCA)及油酸(C18:1n9)均显著缺乏。动物实验证实,口服HDCA能够显著减轻实验性葡萄膜炎小鼠的眼部炎症,降低IL-1β、IL-6等促炎因子水平,同时升高抗炎因子IL-10。机制研究揭示,HDCA在脾脏中高效富集,通过抑制法尼醇X受体(FXR)、激活SREBP1c依赖的脂肪酸合成途径,促进脾脏红髓巨噬细胞生成油酸。油酸经血液循环远程抑制眼部致病性Th17细胞分化,并促进巨噬细胞向抗炎M2表型极化,形成一条全新的"肠道—脾脏—眼"免疫代谢轴。
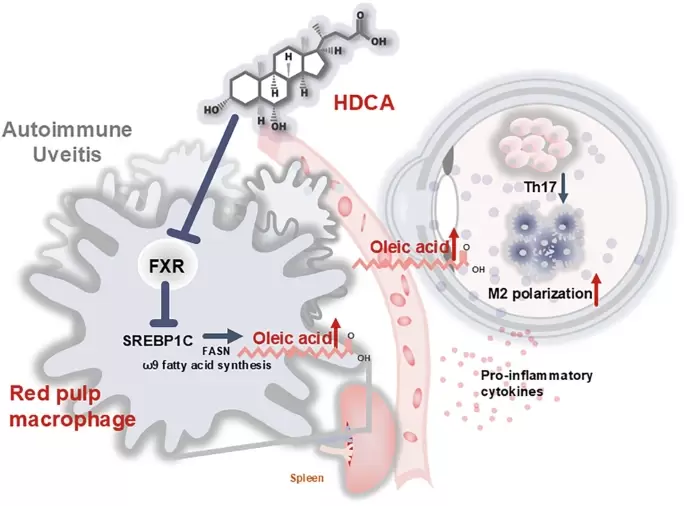
“脾-眼”免疫代谢轴调控示意图。
HDCA作为内源性代谢产物,具有精准靶向、安全性高、可口服给药及成本较低等独特优势,有望成为葡萄膜炎及其他自身免疫性疾病的创新治疗策略。研究团队目前正积极推进临床前安全性评估和制剂研发,力争尽早启动临床试验。
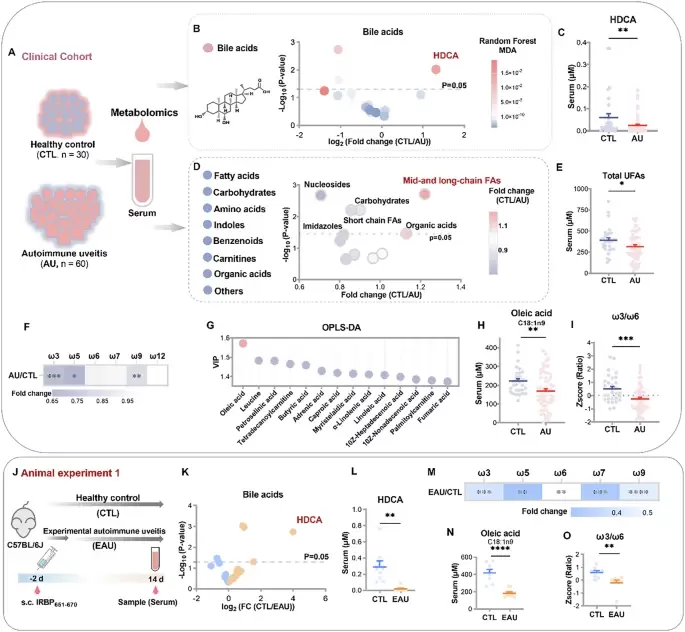
跨物种的 AU 代谢学分析揭示 HDCA 与油酸的不足。
该研究由浸大副校长(研究及拓展)、中医药学院讲座教授吕爱平教授,以及香港大学医学院讲座教授贾伟教授作为共同通讯作者完成,浸大中医药学院李忆涛为共同第一作者。研究获得香港研究资助局优配研究金及上海市科技创新行动计划的资助。
吕爱平教授与贾伟教授多年来共同致力於基於中医药传统,将代谢组学转化为疾病疗法。其合作核心是通过代谢组学鉴定胆汁酸等小分子,开发针对代谢病、癌症等疾病的精准疗法。贾伟教授目前担任浸大访问讲座教授,延续了富有成效的合作,充分体现了浸大"健康与药物研发"跨学科研究集群的核心优势和持续影响力。
上一则消息
02.04.2026
下一则新闻
24.03.2026